(Picture from Duke Today)
안녕하세요 보스턴 임박사입니다.
RNA Therapeutics 중에서 가장 오래된 기술 중의 하나이면서도 발전이 Antisense, siRNA, mRNA 등에 비해서 상대적으로 임상적인 적용이 더디게 진행된 분야가 RNA Aptamer 분야가 아닌가 하고 생각합니다.
이것은 1998년에 FDA에서 승인된 Macugen (Pegaptanib sodium injection)의 상업적 실패와 연관이 있고 Archemix, SomaLogic과 같은 Aptamer 회사들이 문을 닫거나 Research 회사로 Business model이 변화되는 계기가 되었습니다.
다행히도 최근 Iveric Bio/Astellas Pharma의 Izervay (avacincaptad pegol)이 Geographic atrophy 치료제로 FDA 승인이 되면서 RNA Aptamer의 새로운 중흥기가 올 수 있을지 주목되고 있습니다.
The monthly eye injection, which will be sold as Izervay, is meant to slow progression of the condition, which Iveric and its new owner, Japanese drugmaker Astellas Pharma, estimate affects 1.5 million people in the U.S.
Iveric Bio (former Ophthotech Corporation)의 스토리는 Retina Today 2021년에 잘 소개가 되었습니다.
The Open Secret Behind Iveric Bio’s Continued Success – Retina Today 9/1/2021
Baskings Biosciences에 대해 소개를 하려고 합니다.
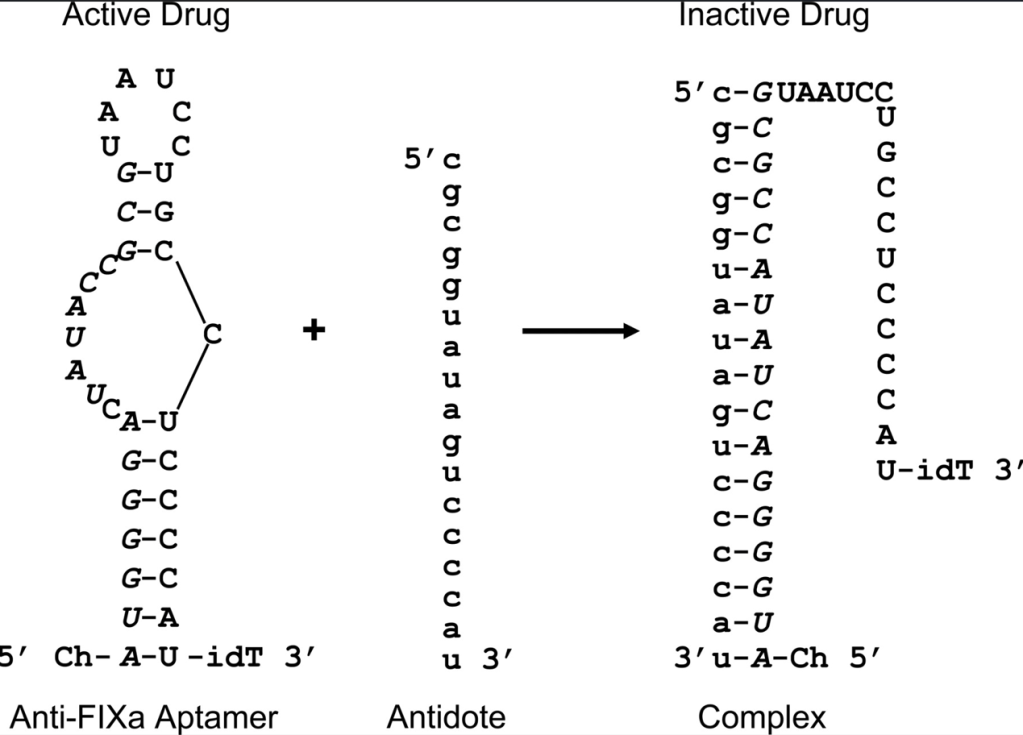
Bruce Sullivan 박사는 25년 이상 RNA Aptamer 분야에서 일한 베테랑 교수인데 2007년에 Oligonucleotides 논문에 von Willebrand Factor를 표적으로 하는 Aptamer 연구결과를 발표한 이후에 이 약물의 성질 변형을 위해 오랜 기간 노력을 해 왔습니다.
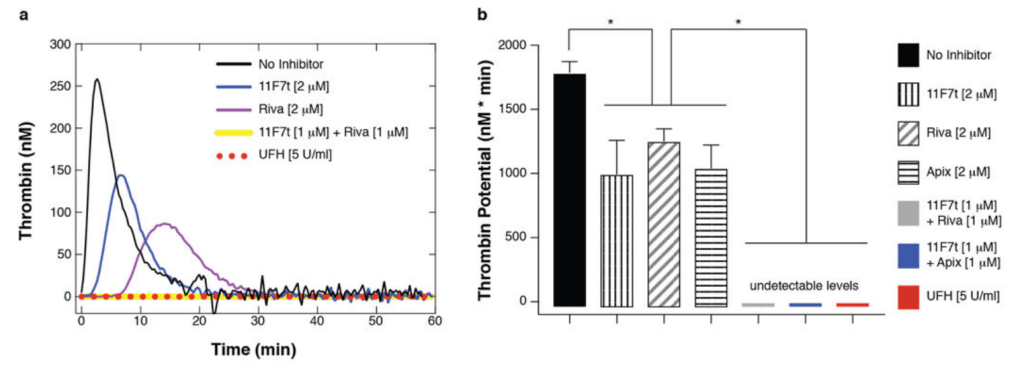
10여년의 연구 끝에 2018년에 Bruce Sullivan 교수는 Nature Biotechnology에 Aptamer와 Oligonucleotide reversal agent combination으로 심장호흡기계의 혈액응고를 방지할 수 있다는 결과를 발표했습니다. RNA Aptamer (11F7t)와 small-molecule FXa inhibitor (apixaban) combination으로 anticoagulation이 잘 되는 것을 발표한 것입니다.
RNA Aptamer의 Renal clearance 문제를 해결하기 위해 주로 PEG conjuagation을 하는데 anti-PEG antibody로 인한 문제가 있었습니다. 그런데 우연인지 거의 같은 시기에 Duke University의 Ashutosh Chilkoti 교수 연구실에서 POEGMA라는 새로운 polymer를 발표합니다.
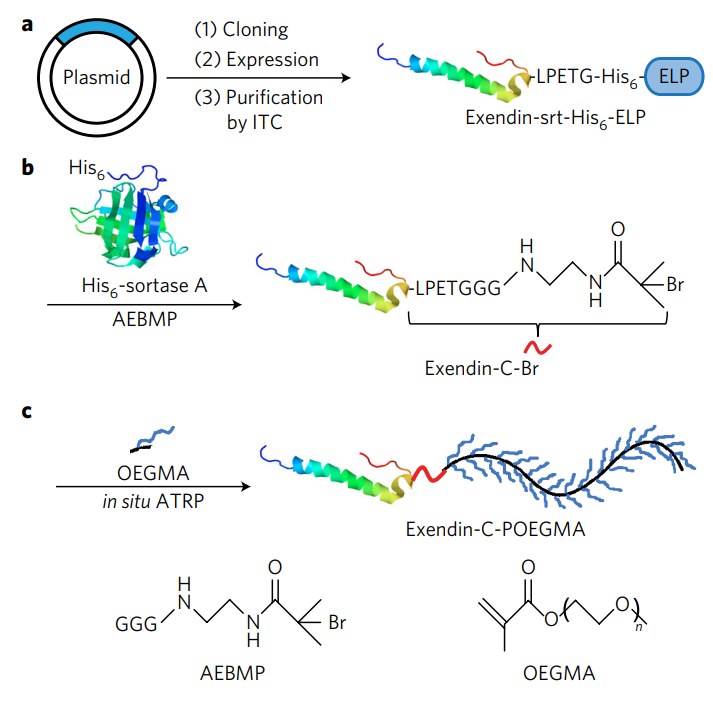
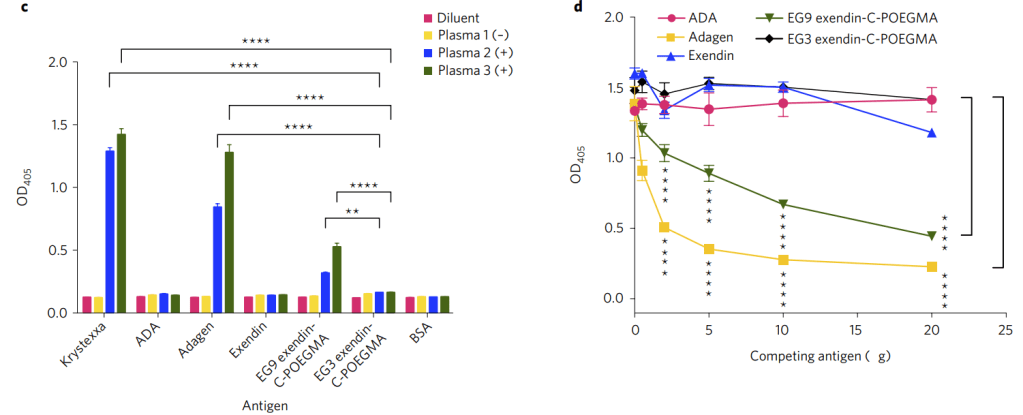
Bruce Sullivan 교수와 Ashutosh Chilkoti 교수는 공동연구를 통해서 POEGMA를 Bruce 교수의 RNA Aptamer에 결합시킨 Aptamer-POEGMA conjuagate의 결과를 발표합니다.
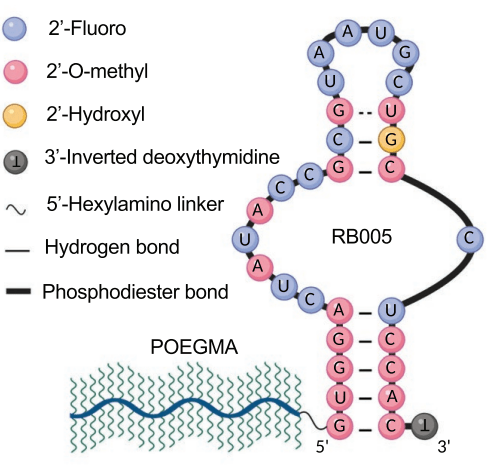
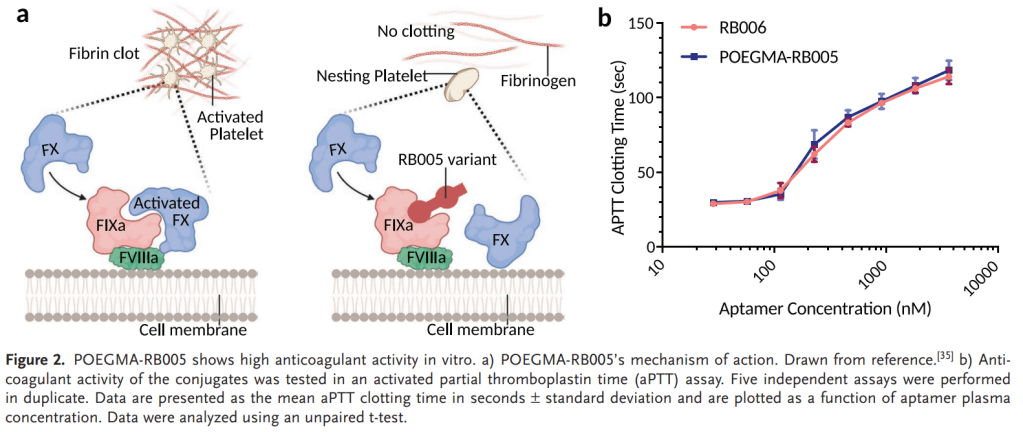
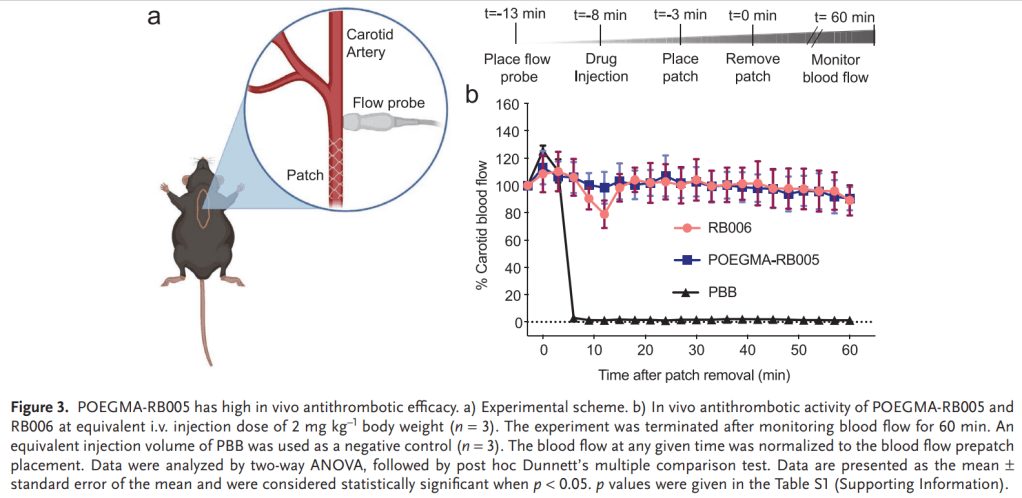
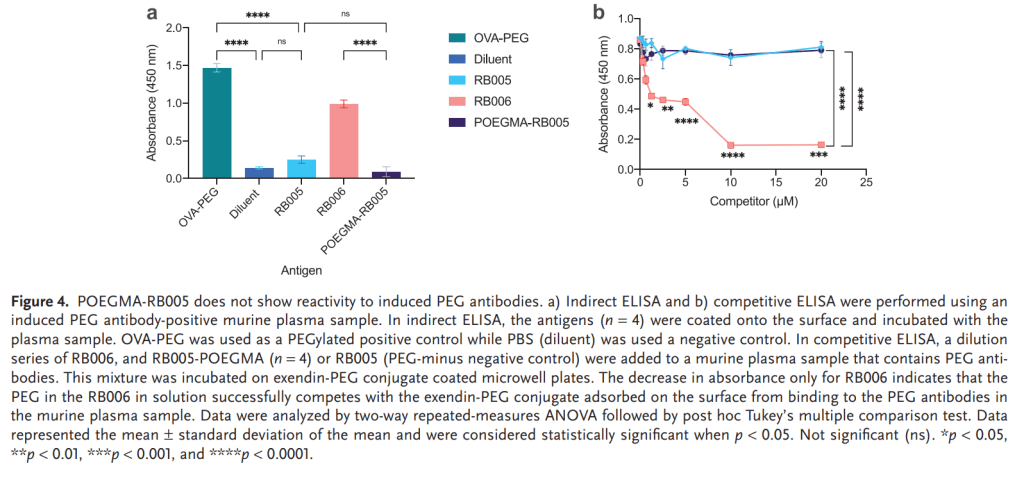
T10으로 부터 T59까지 Truncation optimization을 한 이후에 Antidote를 위해 5개의 Uridine을 넣어서 35-nt Aptamer를 만들었습니다. 이렇게 얻어진 BB-031 (DTRI-031) preclinical development result를 얻었습니다.
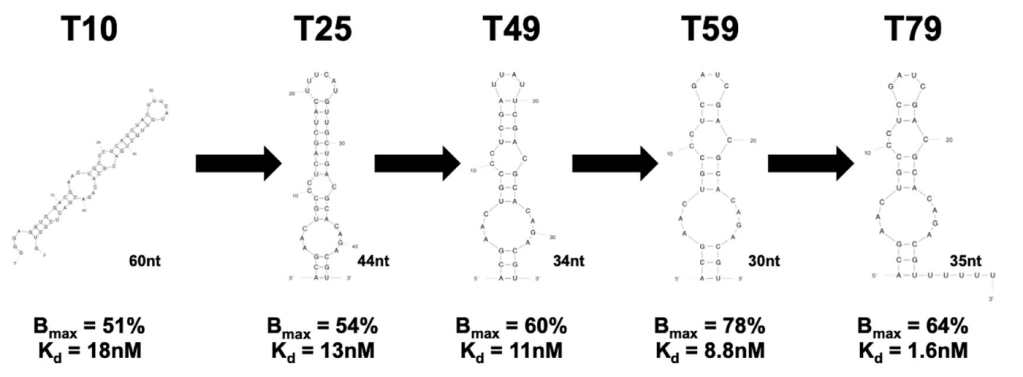
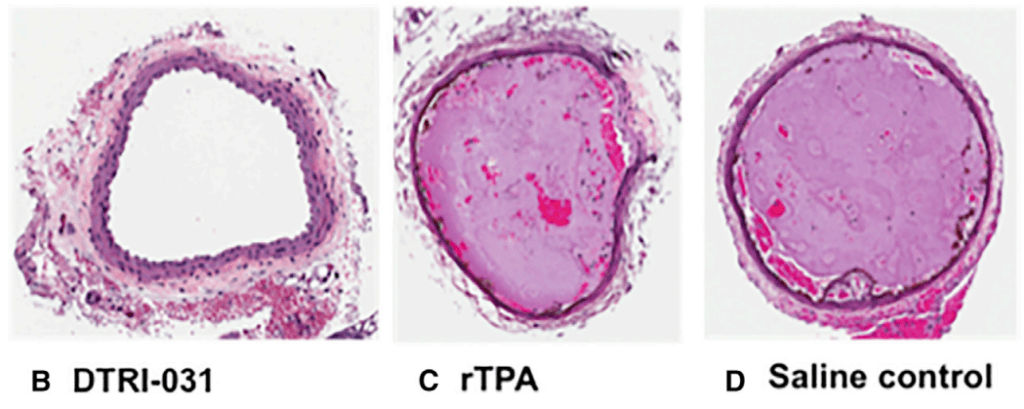
이러한 연구결과를 바탕으로 Bruce A. Sullivan교수와 Shahid M. Nimjee교수는 2019년에 Baskings Biosciences를 창업하였고 1년후에 3개 VC로 부터 $5.4 Million Seed Financing을 받아서 BB-031 (DTRI-031) IND-enabling studies와 phase 1을 지원하게 됩니다.
Basking Biosciences, Inc. Completes $5.4M Seed Financing – Smart Business Dealmakers 12/7/2020
Basking Biosciences, Inc., a privately-held biopharmaceutical company developing a next generation treatment for acute ischemic stroke (AIS), announced an initial closing of a $5.4M Seed Series financing. The investor syndicate includes Rev1 Ventures, Broadview Ventures and Viva BioInnovator. Concurrent with the financing, Ryan Helon of Rev1, Thomas Needham of Broadview and Dr. Dan Meyers have joined Basking’s Board of Directors.
Basking is developing the first reversible thrombolytic therapy for acute ischemic stroke (AIS). The Company’s development candidate, DTRI-031, is an RNA aptamer that inhibits von Willebrand Factor (vWF). Basking is co-developing a matched oligonucleotide reversal agent, DTRI-025, for as-needed, rapid reversal of DTRI-031. Basking’s paired therapy has the potential to significantly expand the population of patients that receives acute thrombolytic therapy by extending the treatment window to 24 hours post stroke onset and aligns well with the urgent need in medicine for precision-based therapeutics in cardiovascular disease. The program is expected to enter into human clinical trials in Q2 2021.
BB-031의 임상 1상 결과는 긍정적으로 나왔습니다. 0.1 mg/kg – 4 mg/kg 용량을 IV 주사제에 대한 28-day SAD 시험 중에서 최대용량까지 큰 부작용이 없었고 18분-61분의 약물 반감기를 보여주었습니다.
Healthy volunteers in the Phase I trial were given BB-031 or a placebo in a 6:2 ratio by intravenous bolus at single ascending doses ranging from 0.1mg/kg to 4mg/kg. It was found that the agent was well tolerated and safe throughout the study period of 28 days, and no significant or treatment-emergent adverse events were reported. Additionally, BB-031 demonstrated an apparent mean terminal half-life ranging from 18 minutes at 0.1 mg/kg to 61 minutes at 4mg/kg.
이러한 고무적인 결과를 바탕으로 최근 Arch Venture Partners 주도 하에 $55 Million Series A를 함으로써 임상2상으로 진입할 수 있게 되었습니다. Arch의 Steven Gillis 박사가 Chair of BOD를 맡고 BB-031의 임상2상 PoC와 reveral oligonucleotide BB-025의 임상1상을 위해 노력하게 됩니다.
Triangle-based Basking Biosciences raises $27.5 million – Business North Carolina 11/15/2023
Basking will initiate a Phase 2 proof-of-concept trial, the RAISE trial, in patients with acute ischemic stroke (AIS) in 2024. In addition to the RAISE trial, Basking will use the funds to advance BB-025, a complementary rapid-acting reversal oligonucleotide capable of quickly neutralizing the pharmacological activity of BB-031, through a Phase 1 clinical program.
BB-031의 임상2상 결과가 어떻게 나올지 궁금합니다. BB-025 Oligonucleotide의 임상진행도 순조롭게 되기를 기대해 봅니다. 현재 Basking Biosciences의 Pipeline은 아래와 같습니다
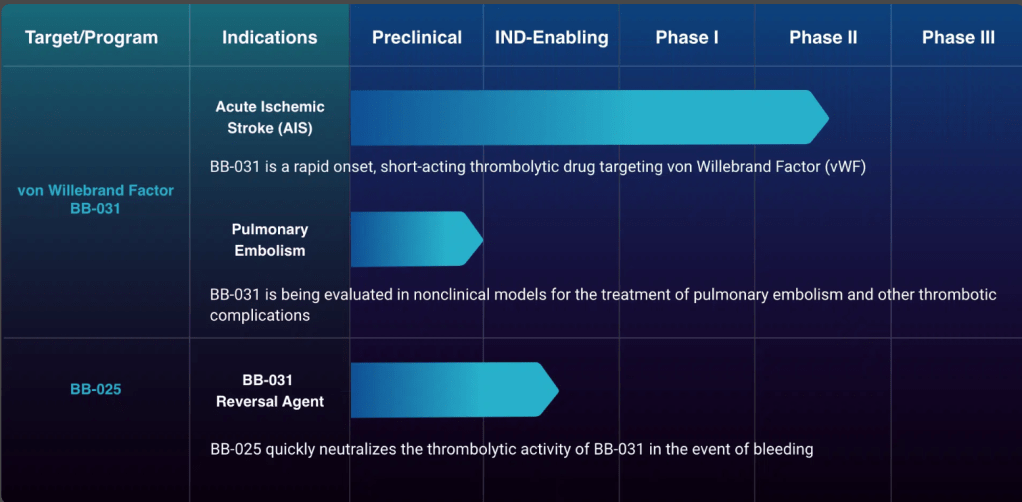
Antidote BB-025에 대한 디자인은 2002년에 Nature에 보고한 바가 있습니다.