
안녕하세요 보스턴 임박사입니다. 최근 Cell therapy 회사인 Vor Bio가 95% 임직원들을 정리해고하면서 정리수순에 접어들었습니다. 이 뉴스는 새로운 유전자 및 세포치료제의 임상시험의 어려움과 함께 현재 펀딩의 어려움이 겹쳐진 결과로 보입니다.
Vor Bio Looks for Exit in Challenging Funding Environment; Lays Off 95% of Staff – Biospace 5/8/2025
회사는 사라지지만 그동안의 Vor Bio의 여정을 정리하고 신규 유전자 및 세포치료제의 개발에 대한 생각들을 나누고자 합니다.
올해 2월에 Vor Bio는 유전자/세포치료제 임상시험에서 환자 등록의 어려움을 보고한 바 있습니다.
“Key findings from the data:
- Educating patients and enrolling them in CGT trials requires more time compared to non-CGT trials due to their complexity and patients’ need for additional reassurance or emotional support.
- Despite the extra time required to educate patients, this did not prevent any survey participants from offering these trials to patients, underscoring the transformative potential of these treatments.
- Study respondents reported that patients share many concerns about CGT trials, including the fear of unknown risks of gene editing and caregiver requirements.”
CGT trials (유전자/세포치료제 임상시험) 과정이 복잡하고 환자들이 새로운 치료제를 받을 것인지에 대한 의사결정을 위해 확신을 갖는 과정이 쉽지 않음을 확인했습니다. 특별히 이것은 유전자 편집기술에 대한 막연한 불안감과 이 치료를 받기 위해 간병인이 필요하다는 등등의 이유로 임상시험이 지속하는데 많은 어려움을 겪고 있었습니다.
“The results reveal significant opportunities for institutions and trial sponsors to improve the patient experience, streamline the process, and enroll more patients in CGT trials. Clinical trial sponsors can address the complexity of cell and gene therapies and help patients better understand these options by providing more comprehensive educational content beyond the handouts typically shared. Additionally, as hospitals are often limited in how many CGT trials they can offer, adding a specialized CGT research team could potentially expand their capacity to offer more trials and treat more patients.”
CGT trials에서 (1) 전체적인 교육내용을 제공하고 (2) 전문적인 CGT 연구팀을 구성함으로써 환자들을 지원해야 한다는 결론에 도달했습니다. 최근에 유전자 및 세포치료제 임상시험은 새로운 유전자 치료의 임상 적용 어려움에 직면하고 있습니다. 이를 위한 충분한 전략이 필요하다고 생각합니다.
Vor Bio는 PureTech Health PLC에서 인큐베이팅한 회사로 2019년에 $42Million Series A를 했습니다.
이 회사는 Columbia University의 Siddhartha Mukherjee교수팀이 2019년 PNAS에 발표한 Gene edited HSC 기술을 기반으로 하고 있습니다.
5AM과 RA Capital이 시리즈A를 주도했고 이사진에 합류했습니다. JJDS와 NIBR도 시리즈 A에 함께 참여했습니다. 시리즈 A를 받았던 2019년 초에는 6명의 임직원이었는데 1년만에 50명까지 규모가 커졌습니다.
시리즈A를 마치고 1년 후에 $110 M 시리즈 B를 마쳤고 VOR33에 대한 임상시험을 준비하기 시작했습니다. 이 당시는 Covid-19 상황이어서 시기적으로 어려운 상황에 성공적인 펀딩을 한 것입니다.
Vor bags $110M to move engineered cell therapy into the clinic – FierceBiotech 07/07/2020
“The series B will push VOR33 into clinical trials in the first half of 2021, a target the company’s on track to meet despite the COVID-19 pandemic. And Vor plans to expand its portfolio beyond CD33, starting with an “umbrella of targets” in the myeloid space, namely in acute myeloid leukemia, myelodysplastic syndromes and related diseases.”
2021년 중순에 Janssen과 공동개발을 하기로 발표를 했습니다.
“Under the terms of the collaboration, Vor Biopharma will investigate the combination of these two technologies into a treatment solution, pairing Vor’s “invisible” eHSC transplant platform with one of Janssen’s bi-specific antibodies in development for acute myeloid leukemia (AML).”
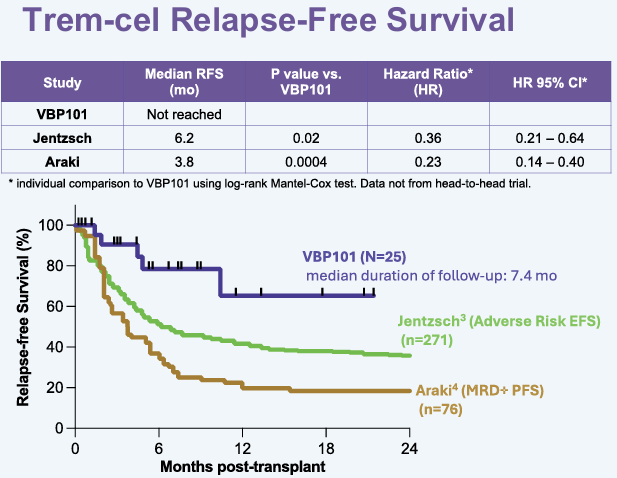
“Preliminary evidence of improved relapse-free survival (median RFS not reached with median follow-up duration of 7.4 months) compared to published groups of AML patients at high risk of relapse post hematopoietic stem cell transplant (HCT)1.
Shielding of the blood system, with maintained neutrophil and platelet counts across multiple Mylotarg doses of 0.5, 1, and 2 mg/m2.
Broadened therapeutic index for Mylotarg when administered after trem-cel.
Reliable engraftment, with 100% of patients achieving primary neutrophil engraftment (median 9.5 days), robust platelet recovery (median 16 days), and full myeloid donor chimerism at Day 28.
Trem-cel continues to be manufactured with high CD33 editing efficiency (median 90%, range 71-94%).”
2024년 12월에 $55.6M의 PIPE 상장을 발표했습니다. 이 때까지 RA Capital이 펀딩에 참여를 했습니다.
Vor Bio Announces $55.6 Million Private Placement – GlobeNewsWire 12/27/2024
“Vor Bio expects to announce updated clinical data from the Phase 1/2 VBP301 trial of VCAR33ALLO in the first half of 2025 and updated clinical data from the Phase 1/2a VBP101 trial of trem-cel in combination with Mylotarg in the second half of 2025.”
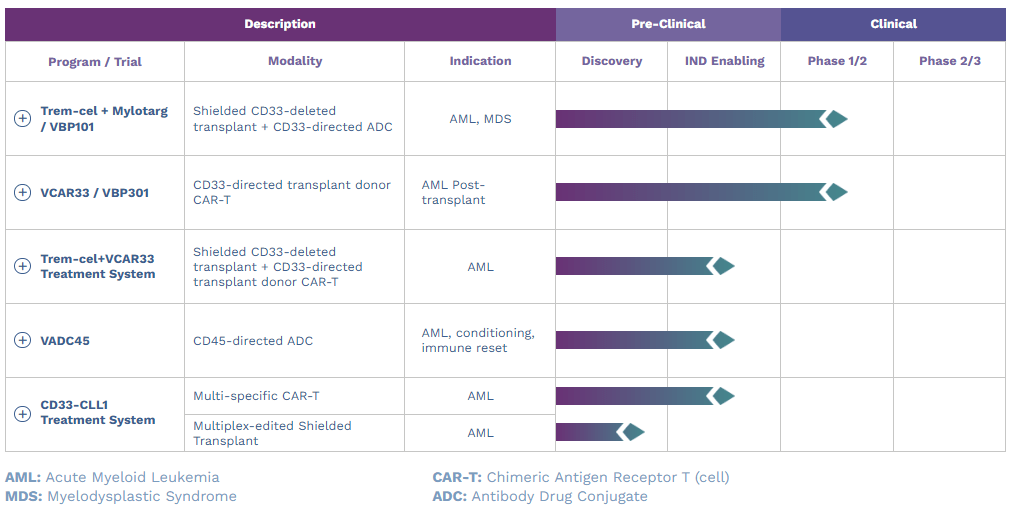
가장 최근의 파이프라인은 ADC, CAR-T 전임상 단계의 파이프라인을 준비하고 있었습니다.
Vor의 기술에서 Cas12a editing에 대해 최근에 발표를 한 결과를 아래에 올립니다.
한달 전 즈음에 Vor Bio의 CSO인 Tirtha의 발표가 있었습니다. Tirtha와는 모더나 초기에 함께 일한 적이 있습니다.
어떻게 보면 Vor Bio는 시기적인 불운도 함께 겹친 것 같은 생각이 듭니다. Covid-19 상황에서 Series B까지 마치고 어려운 임상 환경을 극복하기 위한 노력도 있었던 것 같지만 그래도 PIPE 상장까지 한 이후에 좀 이른 종결을 맺은 것이 아닌가 하는 아쉬움이 남습니다. 그래서 그런지 지금도 Linkedin에서는 Vor Bio의 정리해고 이후 임직원들이 새로운 직장에서 자리를 잡게 하기 위한 동료들간의 의지가 엿보입니다.
Vor Bio의 경우를 보면서 Science 뿐만 아니라 임상 시험의 준비, 그리고 펀딩 등 전략적인 판단이 바이오 벤처 비즈니스에 있어서 얼마나 중요한지 생각해 보는 시간이 된 것 같습니다.
첨부해서 Vor Bio에서 2023년에 CGT 치료제의 FDA clinical holds 현황을 분석한 리뷰가 있어서 첨부합니다. 이것은 유전자 치료제 및 세포 치료제를 연구하는 모두에게 중요한 시사점이 된다고 생각해서 이 곳에 남깁니다.
